Molecular Biology Practical For Honours Fourth Year
Molecular Biology Practical For Honours Fourth Year

Molecular Biology Practical For Honours Fourth Year
Molecular Biology Practical-8 Marks
- Use of Chromatography Technique for Separation of Amino Acid
- Determination of Molecular Weight of Protein molecules using SDS PAGE gel Plates
- Estimation of molecular size of DNA using agarose gel plate.
আণবিক জীববিজ্ঞান ব্যবহারিক(MOLECULAR BIOLOGY practical)




Living Organism-এর বিভিন্ন Molecules-এর গঠন ও কার্যাবলি নিয়ে আলোচনা, পর্যালোচনা ও অধ্যয়নের বিষয় Molecular Biology. ১৯৪৫ সালে William Astbury-Biological Macromolecules-এর ভৌতিক ও রাসায়নিক গঠন বিশ্লেষণ ও ব্যাখ্যা করার ক্ষেত্রে সর্বপ্রথম ‘Molecular Biology’ শব্দটি ব্যবহার করেন। ১৯৫৩ সালে Watson and Crick-এর DNA অণুর দ্বি-সূত্রক, মডেল আবিষ্কারের মাধ্যমেই Molecular Biology-এর মূলভিত্তি শুরু হয়।
প্রােটিন, এনজাইম, কার্বোহাইড্রেট এবং নিউক্লিক অ্যাসিডের (DNA ও RNA) গঠন ও কার্যাবলি-এর অন্তর্গত। বিভিন্ন Bacteriaophage, Virus, E. coli-সহ বিভিন্ন ব্যাকটেরিয়া, এককোষী নীলাভ-সবুজ শৈবাল, ইস্ট, Neurospora-সহ বিভিন্ন ছত্রাক, প্রােটোজোয়া ইত্যাদি Molecular Biology গবেষণায় ব্যবহার করা হয়।
পরীক্ষা নং-১: ক্রোমাটোগ্রাফি পদ্ধতিতে অ্যামাইনাে অ্যাসিড পৃথকীকরণ (Use of Chromatography technique for Separation of Amino Acids)
তত্ত্ব : কোনাে মাধ্যমের মধ্য দিয়ে প্রবহমান দ্রাবকের সাহায্যে একাধিক যৌগের মিশ্রণ হতে যৌগসমূহকে পৃথক করার
পদ্ধতিকে ক্রোমাটোগ্রাফি বলে। আবার পৃথকীকরণ যদি পেপার শিটের উপর বিভিন্ন দূরত্বে ঘটে, তবে তাকে পেপার ক্রোমাটোগ্রাফি বলে এবং এ ধরনের নমুনাকে পেপার ক্রোমাটোগ্রাম বলে। অ্যামাইনাে অ্যাসিড পৃথকীকরণে এই পদ্ধতি ব্যবহৃত হয়।
উপকরণ : বায়ুরােধী সিলিন্ড্রিক্যাল জার, Whatman filter paper No.1, Butanol Acetic Acid Water (BAW- 4: 1: 5) -এর দ্রবণ, মেথিওনিন, লিউসিন, টাইরােসিন, আইসােলিউসিন, ফিনাইল অ্যালানিন প্রভৃতি বিভিন্ন প্রকার অ্যামাইনাে অ্যাসিড, স্কেল, পেনসিল, অ্যাসিটোনে দ্রবীভূত 0.5% নিনহাইড্রিন, হট ওয়াটার বাথ ইত্যাদি।
এই পদ্ধতিতে বিভিন্ন প্রকার অ্যামাইনাে অ্যাসিডের গতির পার্থক্যের কারণে পরস্পর হতে পৃথক হয়ে যায়। প্রতিটি যৌগের জন্য পৃথক পৃথক R-এর মান থাকে, যাকে Resolution font বলে। পরীক্ষায় প্রাপ্ত নির্দিষ্ট যৌগের Rf-এর মান পরিমাপের মাধ্যমে ঐ যৌগকে শনাক্ত করা হয়।
প্রায়ােগিক বিন্দু থেকে কোনাে যৌগের ভ্রমণ দূরত্ব এবং একই সময়ে দ্রবকের ভ্রমণ দূরত্বের অনুপাতকে Rf দ্বারা প্রকাশ করা হয়।
Rf= (প্রায়ােগিক বিন্দু থেকে কোনাে যৌগের ভ্রমণ দূরত্ব ÷ প্রায়ােগিক বিন্দু থেকে দ্রাবকের ভ্রমণ দূরত্ব)
নিম্নে কিছু অ্যামাইনাে অ্যাসিডের Rf-এর মান (BAW-তে) উল্লেখ করা হলাে-
টাইরােসিন- ০.৪৫, মেথিওনিন-০.৫৫, ভ্যালিন-০.৬০, ট্রিপ্টোফেন-০.৫০, লিউসিন-০.৭৩, আইসােলিউসিন-০.৭২, ফিনাইল অ্যালানিন-০.৬৮, লাইসিন-০.১৪।
কার্যপদ্ধতি :
ক. বিউটানল-অ্যাসিটিক অ্যাসিড-পানি (BAW)-৪ : ১ : ৫ অনুপাতে মিশ্রিত করে দ্রাবক তৈরি করে সিলিড্রিক্যাল জারে নেই।
খ, বিভিন্ন প্রকার অ্যামাইনাে অ্যাসিড একত্রে মিশ্রিত করে পানি মিশিয়ে দ্রবণ তৈরি করি।
গ. Whatman filter paper No.1 নিয়ে সিলিড্রিক্যাল জারের উচ্চতার সমান করে এবং জারের ব্যাসার্ধের সমান চওড়া করে কেটে নিই। পেপারের এক প্রান্তে ৩ সে. মি. ভেতরে পেনসিল নিয়ে একটি দাগ দিয়ে তাতে এক ফোটা দ্রব্যের দ্রবণ রাখি। পেপার শুকিয়ে জারের দ্রাবকের উপর খাড়াভাবে এমনভাবে রাখি, যাতে পেপারের গােড়া দ্রাবকের মধ্যে নিমজ্জিত থাকে কিন্তু দাগাঙ্কিত অংশ দ্রাবকের উপরে থাকে এবং পেপারের কোনাে অংশ জারের গাত্র স্পর্শ না করে। এখন দ্রাবক পেপারের ভেতর দিয়ে উর্ধ্বমুখে উঠবে। একে তাই Ascending Paper Chromatography বলে।
ঘ, ৩০ মিনিট পর জার হতে পেপারটি বের করে এনে শুকাই। এ অবস্থায় পেপারটি বর্ণহীন (Undeveloped) দেখায়।
অতঃপর এতে অ্যাসিটোনে দ্রবীভূত ০.৫% নিনহাইড্রিন স্প্রে করে ৮০-১০০° সে. তাপমাত্রায় কয়েক মিনিট উষ্ণ করি।
ফলে অ্যামাইনাে অ্যাসিডগুলাের স্থানসমূহে বর্ণযুক্ত দেখায়। এমন ধরনের ক্রোমােটোগ্রামকে developed বলে। এখন স্কেল ও পেনসিলের সাহায্যে প্রায়ােগিক বিন্দু হতে প্রতিটি দাগের মধ্যবর্তী দূরত্ব পরিমাপ করি।
ঙ, গাণিতিক বিশ্লেষণ
এখানে দ্রাবকের অতিক্রান্ত দূরত্ব =OD
প্রথম দ্রব্যের দ্রাবকের অতিক্রান্ত দূরত্ব =OA
দ্বিতীয় দ্রব্যের দ্রাবকের অতিক্রান্ত দূরত্ব =OB
তৃতীয় দ্রব্যের দ্রাবকের অতিক্রান্ত দূরত্ব =OC
প্রথম দ্রব্যের Rf= (OA ÷ OD) = ০.৪৫, সুতরাং এটি টাইরােসিন।
দ্বিতীয় দ্রব্যের Rf=(OB÷ OD) =০.৫৫, সুতরাং এটি মেথিওনিন।
তৃতীয় দ্রব্যের Rf= (OC ÷OD) = ০.৭২, সুতরাং এটি আইসাে-লিউসিন ।
সাবধানতা : ১। Whatman filter paper No.1. পরিষ্কার ও নতুন হতে হবে।
২. বিউটানল-অ্যাসিটিক অ্যাসিড-পানি (BAW) অনুপাত ৪:১:৫ হতে হবে।
৩, অতিক্রান্ত দূরত্ব সঠিকভাবে পরিমাপ করতে হবে।
৪, সঠিক ও নির্ভুলভাবে develop তৈরি করতে হবে।
পরীক্ষা নংঃ ২ Determination of molecular weight of protein molecules using SDS PAGE gel plates.
তত্ত্ব : প্রােটিনের আণবিক ওজন পরিমাপ করা হয় Polysaccharide slab gel-এ প্রােটিনের electrophoresis দ্বারা।
সুতরাং সরাসরি band pattern তুলনা করা সম্ভব । আদর্শ প্রােটিনের R(value দিয়ে একটি আদর্শ গ্রাফ তৈরির সাহায্যে Rf value (Relative migration value) দ্বারা নমুনা প্রােটিনের আণবিক ওজন পরিমাপ করা যায়।
নিম্নোক্ত সূত্র দ্বারা Rf value হিসাব করা হয়।
Rf= প্রায়ােগিক বিন্দু থেকে প্রােটিনের ভ্রমণ দূরত্ব÷ প্রায়োগিক বিন্দু থেকে reference point এর দূরুত্ব)
উপকরণ : i. ইলেকট্রোফোরাইজড স্ল্যাব জেল ধারণকারী নমুনা প্রােটিন ও মার্কারের band pattern-এর photograph. ii. স্কেল ও iii. গ্রাফ পেপার ।
কার্যপদ্ধতি :
i. প্রায়ােগিক বিন্দু থেকে reference point-এর দূরত্ব সেন্টিমিটারে পরিমাপ করা হলাে এবং তা হলাে 9.0 cm.
ii. নমুনা প্রােটিনের ভ্রমণ দূরত্ব সেন্টিমিটারে নির্ধারণ করা হলাে।
iii. উল্লিখিত সূত্রের সাহায্যে marker এবং নমুনা প্রােটিনের Rf value হিসাব করা হলাে।
iv. Marker প্রােটিনের আণবিক ওজন এবং Rf value দিয়ে একটি গ্রাফ তৈরি করা হলাে।
v. নমুনা প্রােটিনের Rf value দ্বারা গ্রাফ হতে নমুনা প্রােটিনের আণবিক ওজন পরিমাপ করা হলাে-
No of Observation
Name of the Standard Protein
Molecular weight of the standard protein
1
Phosphorylase
94,000 or 94 kd.
2
Bovin Serum Albumin
66,000 or 66 kd
3
Ovalbumin
43,000 or 43 kd
4
Carbonic anhydrase
30,000 or 30 kd
5
Trypsin inhibitor
20,000 or 20.1 kd
6
α-lactalbumin
14,000 or 14 kd
Table
No of Observation
Reference distance (a) (cm)
Migrated distance at standard protein (b) (cm)
Rf value of standard protein
Migrated distance of sample protein cm
Rf Value of sample protein
1
1.2
0.133
1.2
0.13
2
1.7
0.188
1.8
0.20
3
2.9
0.322
2.3
0.25
4
9.0
4.0
0.444
2.9
0.32
5
5.6
0.622
3.3
0.36
6
6.9
0.766
4.0
0.44
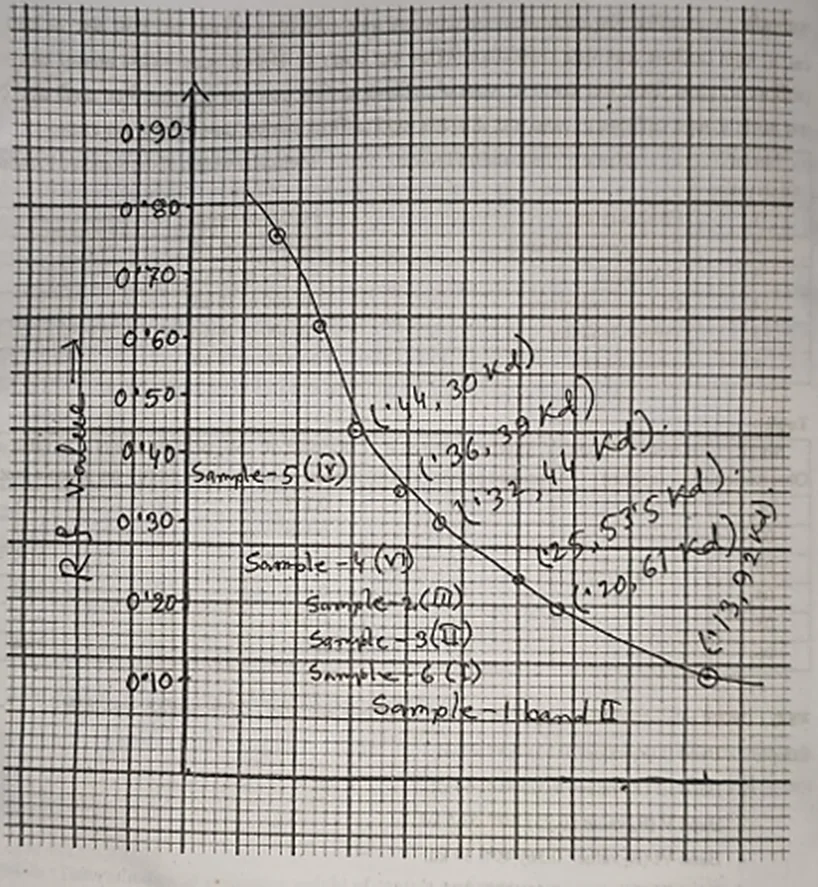
মন্তব্য : জেলের related Protein band থেকে আণবিক ওজন নির্ণয় করা হলাে। নির্ণিত আণবিক ওজন হলাে-
Sample-
1: Band II (Rf value: 0.13) হলাে 92 kd.
2 : Band III (Rf value; 0.32) হলাে 44 kd.
3 : Band v (Rf value : 0.25) হলাে 53.5 kd.
4: Band VI (Rf value : 0.36) হলাে 39 kd,
5: Band IV (Rf value : 0.44) হলাে 30 kd.
6: Band I (Rf value; 0.2) হলাে 61 kd.
সতর্কতা :
i. Slab gel -এ standard protein এবং নমুনা প্রােটিনের অতিক্রান্ত দূরত্ব স্কেল দিয়ে সতর্কতার সাথে পরিমাপ করতে হবে।
ii. প্রােটিনের আণবিক ওজন সতর্কতার সাথে হিসাব করতে হবে।
পরীক্ষা নংঃ ৩: Separation and Identification of Protein by applying PAGE technique (SDS-PAGE Analysis) Poly Acrilamide Gel Electrophoresis কৌশল প্রয়ােগ করে Protein পৃথককরণ ও শনাক্তকরণ।
তত্ত্ব : Agarose আপেক্ষিক স্থানান্তরের নীতিতে একটি electric field আধানযুক্ত DNA, RNA, Protein পৃথক করার কৌশলকে Electrophoresis বলে। একটি Electric field এ আধানযুক্ত DNA, RNA, Protein অণুগুলাে তাদের আধানের প্রকৃতি অনুসারে Cathod বা Anod-এর দিকে ধাবিত হয়।
Gel Electrophoresis -এর Agarose ও Poly Acrilamide ব্যবহৃত হয়। Protein পৃথক করার জন্য SDS-PAGE ব্যবহৃত হয়।
SDS একটি Anionic detergent. SDS দ্বারা Protein-কে বিক্রিয়ান্বিত করা হলে বিকশিত ও ঋণাত্মক আধানযুক্ত হয়। Polypeptide-গুলাে দ্রুত এবং বৃহদাকার অণুগুলাে ধীরগতিতে ধাবিত হয়।Mercaptcethonol Polymeric Protein-এর উপএককগুলাে পৃথক করে ফেলে। প্রমিত Protein-এর সাথে তুলনা করে এবং গতিশীলতার প্রতি ভিত্তি করে পৃথক হয়ে যাওয়া protein অণুগুলাের আণবিক ওজন নির্ণয় করা হয়।
উপকরণ :
যন্ত্রপাতি : Electroforesis যন্ত্র, Micropipette, Pipette নির্দিষ্ট অ্যাম্পিয়ার বিদ্যুৎ সরবরাহ করার জন্য Power pack (-300v) ইত্যাদি।
বিকারক : 30% Acrilamide / bis-Acrilamide (37.5:1) জলীয় দ্রবণ (গাঢ় বর্ণের বােতলে রক্ষিত),
1.5 MTris-HCl বাফার (PH ৪.৪), 0.5 MTris-HCl বাফার (pH 6.8), 10% Amonium Per Sulfate (APS) দ্রবণ (সদ্য প্রস্তুত), Comasi briliant blue (0.3%), TEMED, 10% (W/V) SDS, 1 x Tris – glycine -SDS বাফার (রানিং বাফার), 5X sample বাফার (লোডিং বাফার), পাতিত পানি ইত্যাদি।
কার্যপদ্ধতি (SDS – PAGE Protocol) :
১। Gel Electroforesis যন্ত্রটি সন্নিবিষ্ট করি। Gel plate দুটি ভালােভাবে পরিষ্কার করার পর দু’পাশে স্পেসার (0.8-1.0 mn) বসিয়ে দু’পাশে ও নিচের প্রান্ত রাবার কর্ক দিয়ে বন্ধ করে ক্লিপ দিয়ে আটকে দেই।
২। দুটি পৃথক বিকারে স্ট্যাকির ও সেপারেটিং Gel দ্রবণ তৈরি করে তা মৃদু এবং সম্পূর্ণরূপে নাড়াই।
৩। Pipette-এর সাহায্যে Glass Sandwitch Seperating Gel দ্রবণ দিয়ে পূর্ণ করি। এবার Gel-এর উপরিভাগে পাতিত পানি ঢেলে Polymerization-এর জন্য অপেক্ষা করি। Polymerization সম্পূর্ণ হলে Gel-এর উপরিভাগে এবং পতিত পানির মাঝে একটি স্পষ্ট রেখার সৃষ্টি হয়।
৪। ফিল্টার কাগজের সাহায্যে পানি শুষে নিয়ে Pipette-এর সাহায্যে সদ্য প্রস্তুত স্ট্যাকিং Gel ঢালি।
৫। এবার কূপ (well) গঠনকারী চিরুনির ন্যায় Comb-গুলাে বসিয়ে Polymerization-এর জন্য অন্তত ৩০ মিনিট অপেক্ষা করি। Gel গঠন সম্পূর্ণ হলে Comb-গুলাে সরিয়ে ফেলি। কাচের প্লেটগুলাে কাস্টিং ফ্রেম থেকে তুলে ফেলে Gel-কে Electroforesis ট্যাংকে রাখি। এখন সদ্য প্রস্তুত x Tris – glycine-SDS বাফার দিয়ে ট্যাংক দুটি পূর্ণ করি ।
৬। Protein sample তৈরি করে 2 x sample buffer-এর সাথে 1:1 অনুপাতে মিশিয়ে 95°C তাপমাত্রায় ৫-১০ মিনিট উত্তপ্ত করি। ফলে Protein বিকলিত হয়ে যায়।
৭। Micropipette-এর সাহায্যে কূপগুলাে নমুনা দ্রবণ দিয়ে পূর্ণ করি। প্রথম লেনটিতে protein মার্কার(m) রাখি।
৮। এবার উপরের ঢাকনাটি বসিয়ে বিদ্যুৎ সংযােগ দেই। উপযুক্ত voltage ও ampere যুক্ত (20 mA – 30 mA) বিদ্যুৎ দ্বারা Electroforesis যন্ত্র চালনা করি।
৯। Dye front (Bromfenol blue dye) running Gel-এর নিম্ন প্রান্তে পৌছে গেলে Electroforesis-এর বিদ্যুৎ প্রবাহ বন্ধ করে দেই। Gel Sandwitch-টি বের করে (Staining tray-তে) Rocking shaker-এর ঝাকুনিরত অবস্থায় ২ ঘণ্টা বা সারারাত Gel রঞ্জিতকরণ দ্রবণ দিয়ে রঞ্জিত করার ফলে সম্পূর্ণ Gel নীলবর্ণ ধারণ করে।
১০।Gel-এ destaining দ্রবণ স্থানান্তরিত করে Rocking shaker-এ ৩০ মিনিট ঝাকাই। অতঃপর সদ্যপ্রস্তুত destaining দ্রবণ মিশাই। যতক্ষণ না Gel band-গুলাে স্পষ্টভাবে ফুটে ওঠে, ততক্ষণ পর্যন্ত এই ধাপগুলাে বারবার পুনরাবৃত্তি করি। এই অবস্থায় জেলের ফটোগ্রাফ নেই। জেল স্পষ্টভাবে দেখাগেলে ফটোতােলা জেল বিশ্লেষণ করি।


ফলাফল : Gel-এ কতিপয় নীল রং-এর band স্পষ্টভাবে দেখা যায়।
সাবধানতা :
১। Acrilamide একটি Neurotoxin; তাই এটি ব্যবহারের সময় Gloves, নিরাপদ চশমা এবং sergical musk পরে নিতে হবে।
২। Stacking Gel ঢালার সময় লক্ষ রাখতে হবে, যেন কোনাে বুদবুদ গঠিত না হয়।
৩। Dye front Gel slab-এর নিচে পৌছার সঙ্গে সঙ্গে বিদ্যুৎ প্রবাহ বন্ধ করে দিতে হবে।
৪। APS যােগ করার সঙ্গে সঙ্গে Polymerization শুরু হয়। তাই পরবর্তী কার্যক্রম দ্রুত সম্পন্ন করতে হবে।
বিকারক প্রস্তুত :
১। Stacking Gel – 5ml

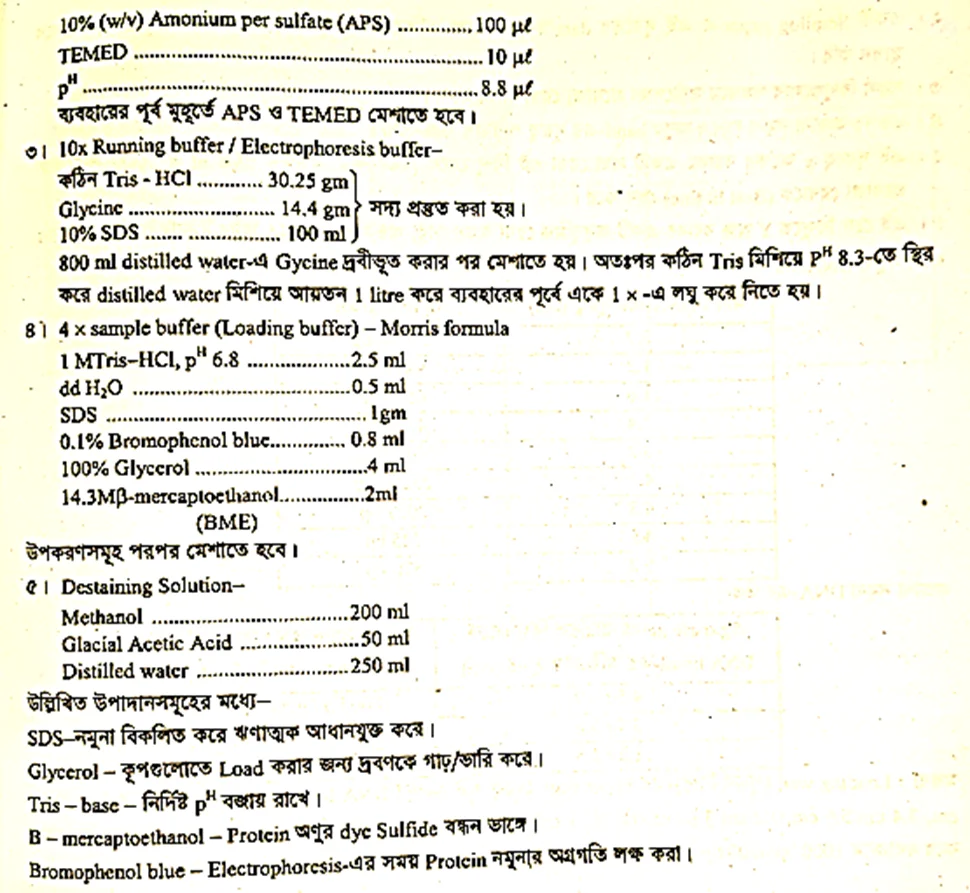
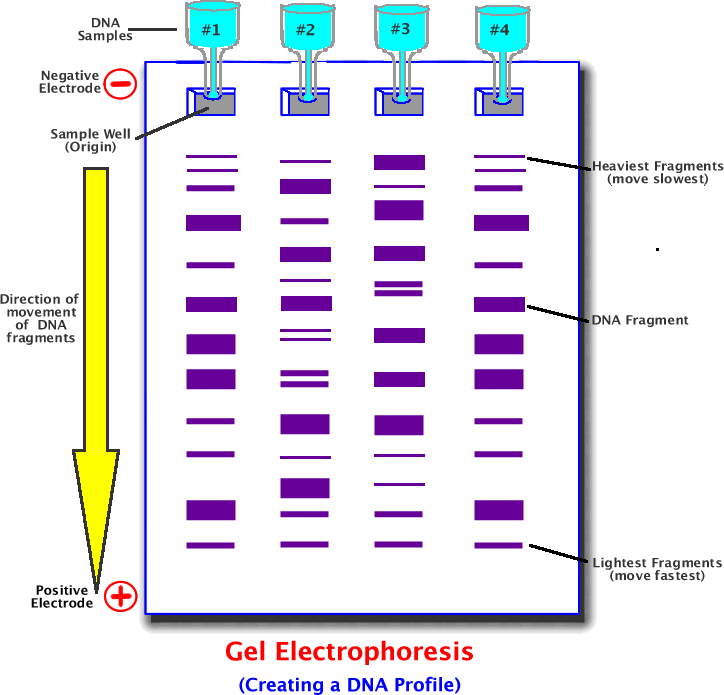
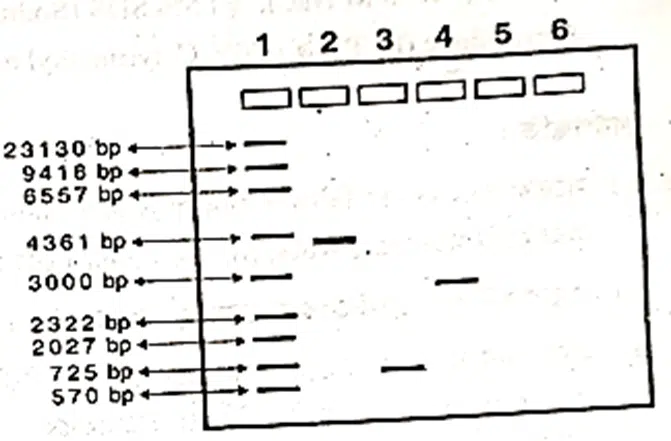
পরীক্ষা নং-৪: Estimation of molecular size of DNA using agarose gel plate.
তত্ত্ব : DNA জীবকোষের বংশগতীয় উপাদান, যা বংশগতীয় তথ্য বহন করে। একটি অজানা DNA অণুর আণবিক আয়তন/দৈর্ঘ্য পরিমাপ করার জন্য দুটি পদ্ধতি রয়েছে। এর জন্য একটি logarithmic phase এবং DNA-এর Gel Electrophoresis ব্যবহৃত হয়।
উপকরণ : একটি Logarithm paper, নমুনা ছবি, পেনসিল, স্কেল ইত্যাদি।
কার্যপদ্ধতি :
১। নমুনা ছবি থেকে Agarose gel-এর loading well-এর প্রায়ােগিক বিন্দু থেকে প্রতিটি DNA band-এর অতিক্রান্ত দূরত্ব সেন্টিমিটারে (cm) পরিমাপ করা হলাে।
প্রতিটি ক্ষেত্রে সবচেয়ে lower, edge-এর নমুনাটিই সবচেয়ে কম দৈর্ঘ্যের DNA band হিসেবে পরিমাপ করা হয়।
২। একটি Semilog paper-এ এই দূরত্বের data/তথ্য x অক্ষে অতিক্রান্ত দূরত্ব এবং Y অক্ষে ক্ষারক জোড় হিসেবে স্থাপন করি।
৩। সকল বিন্দুগুলাের সমন্বয়ে সর্বাপেক্ষা প্রযােজ্য রেখা আঁকা হলাে।
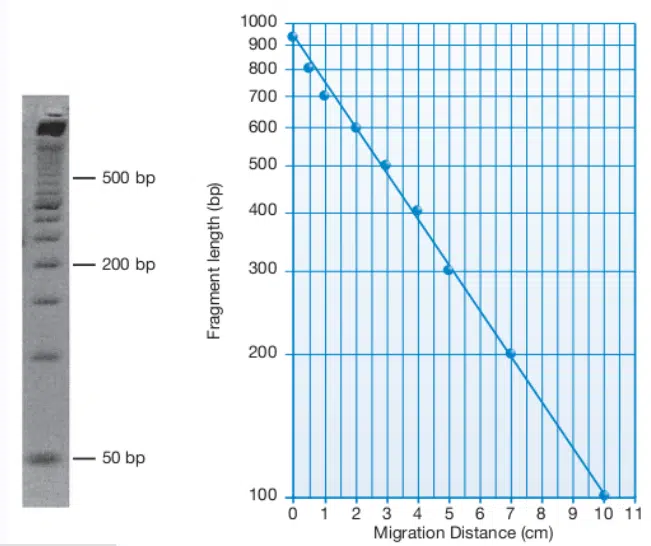
৪। এরপর অজানা নমুনা DNA অণুর band-এর দূরত্ব পরিমাপ করা হলাে।
৫। এই দূরত্বে x অক্ষের বরাবর একটি লম্বা রেখা ওই বিন্দু থেকে অঙ্কন করি, যতক্ষণ পর্যন্ত না এই রেখা সর্বাপেক্ষা প্রযােজ্য রেখাকে (Best lit fine) ছেদ করে।
৬। এই ছেদ বিন্দুতে Y অক্ষ বরাবর একটি অনুভূমিক রেখা অঙ্কন করি, যার মাধ্যমে DNA অণুর নমুনার দৈর্ঘ্য মাপা হয়।
জানা নমুনা DNA-এর তথ্য
আদর্শ DNA-এর দূরত্ব (cm)
আণবিক ওজন
0.7
23130 bp
1.2
9416 bp
1.6
6557 bp
2.4
4361 bp
3.2
3000 bp
4.1
23200 bp
4.3
2027 bp
4.9
725 bp
5.2
570 bp
অজানা নমুনা DNA-এর তথ্য
Agarose gel-এ প্রারম্ভিক বিন্দু থেকে DNA band-এর অতিক্রান্ত দূরত্ব (cm)
অজানা নমুনা DNA অণুর আণবিক আয়তন/দৈর্ঘ্য
4.5/2.9
1000 bp/ 4200 bp
3.4/5.6
2500 bp/ 2650 bp
1.2/3.8
15,500 bp / 2400 bp
মন্তব্য : Loading well (সূচনা বিন্দু)-এর lower edge থেকে ৩টি অজানা DNA band-এর দূরত্ব যথাক্রমে 4.5 cm/2.9 cm, 3.4 cm/5.6 cm, 1.2/cm 3.8 cm-এই ৩টি band-এর আণবিক আয়তন/ওজন logarithmic গ্রাফ পেপার ব্যবহার করে যথাক্রমে 1000 bp/4200 bp, 2500 bp/2650 bp এবং 15500 bp/2400 bp পরিমাপ করা হলাে।
Molecular Biology Practical For Honours Fourth Year
পরীক্ষা নং- ৫: DNA Isolation/Extraction by CTAB method (CTAB পদ্ধতিতে DNA পৃথকীকরণ/নিষ্কাশন) ।
তত্ত্ব : DNA fingerprinting, Genetic recombination এবং অন্যান্য Genomic বিশ্লেষণের জন্য DNA পৃথকীকরণ/ নিষ্কাশন প্রয়ােজন। DNA পৃথক করার বেশ কয়েকটি পদ্ধতি রয়েছে। তার মধ্যে CTAB পদ্ধতিতে (Cetyrimethyl ammonium bromide) DNA নিষ্কাশন সহজ ও সংক্ষিপ্ত পদ্ধতি।
উপকরণ :
ক. যন্ত্রপাতি :
১। Microcentrifuse, ২। Morter & Pestle, ৩। Incubator ৪। Autoclave, ৫। Balance, ৬। Eppendorf (ঢাকনাযুক্ত ছােট প্লাস্টিকের টিউব) ৭। Micropipette ইত্যাদি।
খ. বিকারক : ১। Extraction buffer, ২। TE buffer, ৩। Phenol; Chloroform; Isoamyle alcohol, ৪। 70% Ethanol, 16 M NaCl, ৬, 5% SDS (Sodium Dodecyle Sulphate) ৭, Isopropanol, ৮, 10% Polyvinyl Pyrrolidone (PVP). ৯, 20% Cetyrimethyl ammonium Bromide (CTAB) ইত্যাদি।
কার্যপদ্ধতি :
১। সতেজ Stevia-এর বিটপ শীর্ষের অংশ এবং পরিণত পাতা 1 cm করে টুকরা করে 0.2 gm Autoclave-এ নির্বীজিত করা ছােট মর্টার ও পেস্টলে (6.5 x 2.5 cm) রেখে 800 μl Extraction buffer মেশাই।
২। এবার মর্টার ও পেস্টলের সাহায্যে চূর্ণ করে মিহি কণায় পরিণত করি।
৩। এবার চূর্ণ করা নমুনা 2ml Eppendorf টিউবে নিই। অতঃপর এর সাথে 150 μl 50% SDS, 150 μl 10% PVP এবং 150 al 20% CTAB মিশিয়ে ভালােভাবে মিশ্রিত করি। তারপর একে 65°C তাপমাত্রায় water bath-এ ৪০ মিনিট incubate করি। এ সময় ৩-৪ বার মিশ্রণটি ভালােভাবে মিশাই।
৪। Waterbath থেকে নমুনা বের করে কক্ষ তাপমাত্রায় ঠান্ডা করি। অতঃপর এর সাথে সমপরিমাণ Phenol ;Chloroform : Isoamyle alcohol (25 : 24 : 1) যােগ করে ভালােভাবে মেশাই। এবার একে কক্ষ তাপমাত্রায় 10000 rpm-এ ৩০ মিনিট সেন্ট্রিফিউজ করি।
৫। এখন জলীয় অংশ (প্রায় ৪00 μl) পৃথক করে একটি নতুন বরফ শীতল 2 ml Eppendorf টিউবে রাখি। এর সাথে প্রথমে সমপরিমাণ বরফ শীতল Isopropanol এবং তারপর 120 μl 6M NaCl যােগ করি। অতঃপর-একে 20°C তাপমাত্রায় ১ ঘণ্টা Incubate করে তারপর 10,000 rpm-এ ২০ মিনিট Centrifuge করি।
৬। এবার Adjustable micropipette-এর সাহায্যে দ্রবণের উপরের স্তরটি পৃথক করে ফেলি। অতঃপর 2.5 গুণ 70% বরফ-শীতল Ethanol যােগ করে কক্ষ তাপমাত্রায় 10,000 rpm-এর ১০ মিনিট Centrifuse করি।
৭। পিলেট গঠিত হলে টিউব থেকে সাবধানে দ্রবণটি ফেলে দেই। এবার 70% Ethanol টিউবের নিচু অংশ পর্যন্ত যােগ করি।
৮। টিউব থেকে সাবধানে Ethanol ঢেলে ফেলি। এখন টিউব উলটা করে ৩০ মিনিট একটি ফিল্টার পেপারের উপর পিলেট শুকিয়ে নিই। এখন 50 μl TE buffer ঢেলে DNA পিলেটগুলাে ডুবিয়ে রাখি। এবার একে-20°C তাপমাত্রায় সংরক্ষণ করি।
সতর্কতা :
১। নিষ্কাশন প্রক্রিয়ার সময় এবং রাসায়নিক দ্রব্য কাজ করার সময় হাতে Gloves পরে নিতে হবে।
২। স্টক দ্রবণ তৈরির সময় দ্রবণের pH অত্যন্ত সাবধানে সঠিকভাবে নির্ণয় করতে হবে।
৩। নমুনা সংগ্রহে বিশেষ সতর্কতা অবলম্বন করতে হবে।
স্টক দ্রবণ প্রস্তুতকরণ-
১। 1M Tris HCI -এর স্টক দ্রবণ (pH 8.0)-
12: 11 gm Tris base 75 ml distilled water পানিতে দ্রবীভূত করি। ড্রপারের সাহায্যে 5.5 ml 10NH4Cl ধীরে ধীরে মিশিয়ে দ্রবণের pH8.0 স্থির করি। এবার দ্রবণটি কক্ষ তাপমাত্রায় কয়েক মিনিট রেখে তারপর অবশিষ্ট distilled মিশিয়ে আয়তন 100 ml করে Autoclave-এ নিবীজিত করে 4°C তাপমাত্রায় সংরক্ষণ করি।
২। 0.5 M EDTA স্টক দ্রবণ (pH8.0)–
18.61 gm EDTA 75 ml distilled water-এ মিশিয়ে Magnetic sterer-এর সাহায্যে আলােড়িত করে তারপর 2 gm NaOH বিশুদ্ধ, পিলেট মিশিয়ে দ্রবণের pH 8.0 স্থির করি। এতে EDTA ভালােভাবে দ্রবীভূত হয়। এখন Distilled water মিশিয়ে আয়তন 100 ml করে Autoclave-এ নিবীজিত করে 4°C তাপমাত্রায় সংরক্ষণ করি।
৩। 6M NaCl স্টক দ্রবণ-
200 ml distilled water-এ 87.66 gm NaCI দ্রবীভূত করে তারপর distilled water মিশিয়ে আয়তন 250 ml করে Autoclave-এ নির্বীজিত করে 4°C তাপমাত্রায় সংরক্ষণ করি ।
৪। 5% SDS-এর স্টক দ্রবণ
5gm SDS 75 ml distilled water -এ দ্রবীভূত করে মিশ্রণটি 65°C তাপে হালকাভাবে ঝাকিয়ে তারপর distilled water মিশিয়ে আয়তন 100 ml করি।
৫। 10% PVP স্টক দ্রবণ-
10 gm PVP 75 ml distilled water-এ দ্রবীভূত করে distilled water মিশিয়ে আয়তন 100 ml করে 4°C তাপমাত্রায় সংরক্ষণ করি।
৬। 20% CTAB স্টক দ্রবণ-
75 ml distilled water-এ 20 gm CTAB পাউডার দ্রবীভূত করে distilled water মিশিয়ে আয়তন 100 ml করে কক্ষ তাপমাত্রায় সংরক্ষণ করি।
৭। TE buffer (pH 8.0) স্টক দ্রবণ
0.2 ml (200 ul) 0.5 M EDTA-এর সাথে 1 ml 1 M Tris HCl যােগ করি। Distilled water মিশিয়ে আয়তন 100 ml করি। 0.45 l ছিদ্রযুক্ত disposable Filter sterilizer-এর সাহায্যে নিবীজিত করে 4°C তাপমাত্রায় সংরক্ষণ করি ।
৮। TE সম্পৃক্ত Phenol-
একটি টেস্টটিউবে spatula-র সাহায্যে কয়েকটি phenol-এর স্ফটিক নিয়ে একটি water bath-এ 65°C তাপমাত্রায় ১৫ মিনিট ফোটাই। এবার একটি 250 ml বিকারে 40 ml গলিত phenol-এর সাথে সমপরিমাণ TE buffer যােগ করি। এখন Magnetic stirrer-এর সাহায্যে ১০ মিনিট আলােড়িত করে ৫ মিনিট স্থিরভাবে রেখে দেই। ফলে তরলটি উপরে বর্ণহীন ও নিচে বর্ণযুক্ত এদুটি স্তরে পৃথক হয়ে যায়। একটি ড্রপারের সাহায্যে উপরের বর্ণহীন স্তরটি ফেলে দিয়ে 40 ml TE buffer মিশিয়ে পুনরায় উপরের স্বচ্ছ স্তরটি ফেলে দিয়ে নিচের স্তরটির pH 6–7.8-এ পৌছা পর্যন্ত অন্তত ৬ বার প্রক্রিয়াটি চালিয়ে যাই। এতে ৩ ঘন্টা ৩০ মিনিট সময় লাগতে পারে। এই দ্রবণ তৈরির সময় অ্যাপ্রন,গ্লোভস ও মাস্ক পরে নিতে হবে।
৯। Phenol : Chloroform : Isoamyle alcohol 19 (25 : 24 : 1)
50 ml দ্রবণ তৈরির জন্য 25 ml সম্পৃক্ত Phenol 24 ml Chloroform ও 1 ml Isoamyle alcohol ভালােভাবে মিশিয়ে 4°C তাপমাত্রায় সংরক্ষণ করি।
১০। Extraction buffer (Homogenization buffer)-
1M Tris HCl (pH 8.0)———– 2ml
0.5 M EDTA (pH 8.0)———–1 ml
6M NaCl ————————– 3.6 ml
20% CTAB ———————–0.2gm
0.06% Sodium Sulphite——-0.0060 gm
dd H2O————————- 3.124 ml
10 ml দ্রবণ তৈরিতে উল্লিখিত উপকরণগুলাে পরপর মিশাতে হবে। CTAB মেগানাের পূর্বে water bath-এ 650C তাপমাত্রায় উত্তপ্ত করে নিতে হবে এবং ব্যবহারের পূর্ব মুহূর্তে sodium sulphite যােগ করতে হবে। সদ্য তেরি Extraction buffer ব্যবহার করতে হবে।
এই buffer-এর বিভিন্ন উপাদানের কাজ নিম্নরূপ-
Tris HCl-pH বজায় রাখে। EDTA-DNAse-এর কার্যকারিতা রুদ্ধ করে এবং Ca++ ও Mg++ আয়নকে আবদ্ধ (chelate) করে।
NaCI-Polysaccharide মুক্ত করে। CTAB-টিস্যু দ্রবীভূত করে এবং Sodium sulphite-phenol-এর জারণ প্রতিহত করে।
Read more: Biotechnology and Genetic Engineering Practical for Honours Fourth year









